2025-09-19
深部脑刺激(DBS)精准干预
深部脑刺激(DBS)作为一种经美国食品药品监督管理局(FDA)批准的成熟技术,已成为帕金森病(PD)治疗的重要手段。对于那些药物治疗效果不佳、存在难以控制的震颤、明显运动波动或药物引起的运动障碍的患者,DBS能显著改善生活质量。
然而,DBS治疗的成功离不开精准的患者选择、合适的靶点定位、先进的硬件支持以及个性化的编程策略。今天,我们就来详细解读这一技术如何为帕金森病患者带来希望。
谁适合接受DBS治疗
DBS治疗的第一步,是通过多学科团队的全面评估筛选合适的患者。这个团队通常包括神经科医生、神经外科医生、精神科医生、神经心理学家、康复科医生,甚至社会工作者,他们共同评估手术的风险与收益,确立治疗目标。
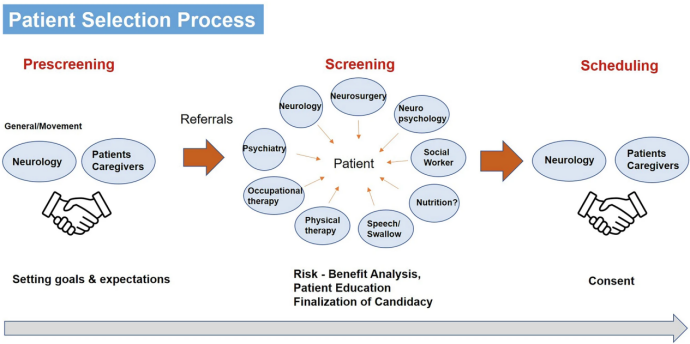
图一:DBS患者选择过程的工作流程:DBS的潜在考虑首先在临床上启动。下一步是由神经科医生、神经外科医生、精神科医生、神经心理学家、康复学科和社会工作者组成的团队进行跨学科评估,以讨论个体患者的风险和益处,提供教育并最终确定候选资格。所选候选人的最后一步是安排手术。
核心评估标准
临床上,晚期帕金森病患者可参考“5-2-1标准”:每天需口服左旋多巴≥5次,同时每天有≥2小时的“关”期症状和≥1小时的困扰性运动障碍。此外,对药物显著不耐受、药物难治性肌张力障碍或运动功能恶化影响就业的患者,也可考虑DBS或其他器械辅助治疗(如左旋多巴-卡比多巴输注泵)。
关键考量因素
年龄:生理年龄比实际年龄更重要。虽然多数中心认为70-75岁以下患者更适宜,但研究显示,75岁以上患者也能从中获益,且90天并发症风险与年轻患者相似。
性别与种族:帕金森病在男性中更常见,但女性运动障碍风险更高,且接受DBS的比例偏低,可能与照顾责任、职业职责等有关。种族差异也较明显,黑人、西班牙裔患者接受DBS的可能性显著低于白人,需加强针对性咨询与支持。
左旋多巴反应性:术前左旋多巴激发试验中,运动评分下降≥30%(尤其50%左右)预示更好预后,尤其对丘脑底核(STN)-DBS患者。但即使反应不佳,若震颤严重,DBS仍可能有效。
轴性症状:如步态冻结、姿势异常、言语障碍等,对左旋多巴反应较差。长期随访发现,STN-DBS对轴性症状的疗效可能逐渐减弱,术前评估需谨慎。
非运动症状:包括认知、抑郁、睡眠障碍等,虽DBS可能改善部分症状,但需提前与患者沟通预期,避免不切实际的期望。
遗传因素:LRRK2、GBA1等基因突变会影响DBS效果。例如,LRRK2-G2019S变异患者对STN-DBS反应较好,而GBA1突变患者可能面临术后认知下降风险。
手术时机:EARLY-STIM试验表明,病程≤4年、出现运动并发症时早期干预,可预防残疾、提高生活质量,但需注意排除非典型帕金森综合征。
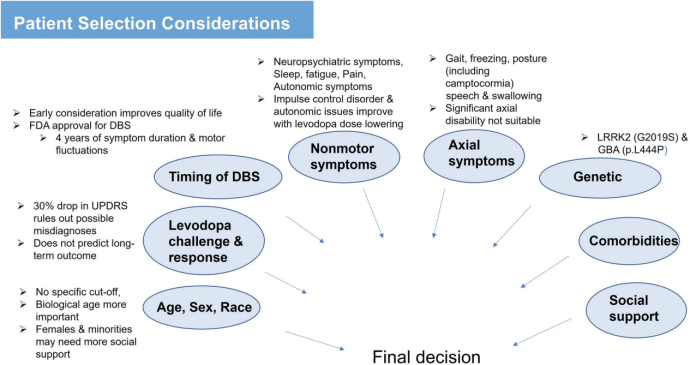
图2:DBS患者选择涉及的因素包括年龄、性别、种族、左旋多巴反应性、手术考虑的时机、轴向和非运动症状负担、遗传因素、合并症和社会支持。
靶点选择:STN与GPi各有千秋
DBS的疗效与靶点选择密切相关,丘脑底核(STN)和苍白球内侧部(GPi)作为帕金森病深部脑刺激(DBS)的两大核心靶点,在临床应用中展现出不同的优势,同时,其他潜在靶点仍在研究中。
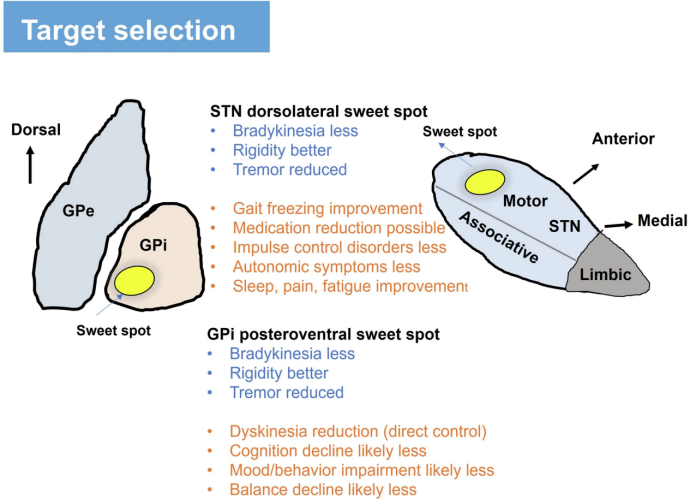
图3:丘脑底核(STN)和梅毒球内(GPi)是两个主要的DBS靶标。导致症状最佳控制的最佳点位于背外侧STN和后腹侧GPi。以蓝色列出的运动迟缓、强直和震颤症状与针对STN和GPi的DBS的发生程度相似。特定靶点的临床益处以橙色列出。
丘脑底核(STN)的核心优势
显著减少多巴胺能药物剂量:双侧STN刺激可使患者的多巴胺能药物剂量大幅降低,多数研究中减少幅度达50%以上。例如,在NSTAPS研究中,患者的左旋多巴等效日剂量(LEDD)从基线时的约1200毫克降至3年时的约600毫克;另一项针对49例接受双侧STN-DBS治疗的患者的5年前瞻性研究显示,左旋多巴等效日剂量从基线时的约1400毫克显著降至5年随访时的约500毫克。这种药物减量能有效解决左旋多巴诱发的过度不自主运动、多巴胺失调综合征及冲动控制障碍等并发症,尤其对年轻患者更为重要。
全面改善运动症状:STN-DBS对运动迟缓、僵硬、震颤等核心运动症状的控制效果显著。尽管大规模研究表明STN与GPi在运动迟缓与僵硬的长期改善上效果相似,但有研究指出,STN-DBS在关期运动迟缓的改善程度上略优于GPi。
历史应用优势:由于早期研究认为双侧STN刺激能更持久地控制症状、疗效衰减较少,因此在临床实践中曾更受青睐。
苍白球内侧部(GPi)的核心优势
直接抑制异动症:GPi-DBS能直接且显著地改善异动症,改善幅度可达60%至70%,这是STN-DBS未观察到的效果,因此对异动症严重的患者尤为适用。
对认知和情绪影响较小:相较于STN-DBS,GPi刺激对认知功能(如言语流畅性、visuomotor处理速度)和情绪的负面影响更小,更适合担心术后认知下降或存在情绪障碍风险的患者。
编程更简便:GPi靶点的编程方法相对简单,且与更好地维持步态和认知功能相关,能减少临床操作的复杂性。
此外,在震颤控制方面,STN和GPi-DBS的效果相当,但部分严重震颤患者可能需要联合腹中间核(Vim)等靶点以增强疗效。
靶点定位技术
神经影像学:3T/7TMRI、定量磁敏感图等提升靶点可视化精度,7TMRI可显示更小核团;扩散张量成像帮助定位相关白质纤维束,优化刺激效果。
微电极记录(MER):通过记录神经元活动确定靶点边界,结合局部场电位(LFP)分析,提高定位准确性,减少主观偏差。
精准治疗的硬件支撑
深部脑刺激(DBS)硬件的发展是帕金森病精准治疗的重要保障。目前,多家厂商的技术竞争推动着设备在精准性和适用性上不断升级。
电极设计方面,传统四极电极可覆盖丘脑底核、苍白球内侧部等常规靶点,但灵活性有限。新型定向电极含16个触点,中间触点分为3个120°扇形分段,能精准调控电流方向,降低刺激剂量40%以上,扩大治疗窗口,减少并发症,尤其适合复杂靶点。多触点线性电极支持多靶点治疗,如8触点电极可同时改善震颤与步态问题。
植入式脉冲发生器(IPG)中,不可充电型寿命3-5年,需频繁手术更换;可充电型寿命达15年以上,部分型号达25年,能减少手术次数,节省成本,但瘦体型患者可能面临皮肤糜烂风险。93.8%的用户认为可充电IPG充电“容易”,每周约需2小时。
多数设备在特定条件下可进行3.0TMRI,部分型号支持“开机扫描”。设备可及性受地域影响,部分系统主要在亚洲销售,选择需结合当地条件及医疗团队熟悉度。
从经验到智能,精准调控“恰到好处”
DBS编程是优化疗效的关键,传统方法依赖经验,耗时且易过度刺激,如今技术革新正实现“精准剂量”治疗。
定向编程通过分段触点调控电流方向,降低刺激剂量40%以上,减少言语不清等副作用。图像引导编程结合术前MRI与术后CT构建3D模型,像“GPS”般快速定位参数,将编程时间从45分钟缩至20分钟,同时可视化刺激范围。
远程编程便捷性显著,相关平台支持远程调整参数,方便偏远患者,但需注意,患者自我调整可能延长治疗时间或增加副作用,需加强教育。
传感技术是重要突破,新型设备可记录局部场电位(LFP),其中β频段反映运动迟缓,γ频段关联异动症,为编程提供客观依据。自适应DBS(aDBS)能实时监测神经信号,动态调整参数,节能40%-70%,2025年获批的相关系统适合震颤、运动波动患者,在提升疗效的同时减少不必要干预。
DBS迈向精准化、个体化
帕金森病DBS治疗的成功,依赖于多学科团队的精准评估、合适的靶点选择、先进的硬件支持及智能编程策略。从患者筛选时的生理年龄、遗传背景考量,到靶点定位的影像与电生理结合,再到硬件的个性化选择和编程的智能调控,每一步都在向“精准医疗”迈进。
随着技术的不断革新,DBS将为更多帕金森病患者带来更安全、有效的治疗,改善生活质量。但需注意,治疗效果仍需长期随访验证,医患共同决策、个性化方案制定仍是核心。
https://mp.weixin.qq.com/s/JYklb2GMYmpYf1vgobXg5Q